

FLT3是成人和兒童AML患者中最常見的突變基因,FLT3是III類受體酪氨酸激酶家族的成員,FLT3抑制劑Midostaurin(咪朵妥林)和gilteritinib(吉列替尼)已被批準用于FLT3突變的急性髓系白血病(acute myeloid leukemia ,AML)。咪朵妥林聯合標準化療的療效顯著,推動人們不斷探索更多新的、更有效的靶點抑制劑(包括吉列替尼)作為聯合化療的一線用藥。同時,在FLT3突變的復發性/難治性AML患者中,吉列替尼和其他新的FLT3抑制劑單一療法較挽救性化療的療效和安全性更好,但一部分FLT3突變的患者對吉列替尼無應答或產生耐藥性。FLT3抑制劑與低甲基化藥物聯合用于造血干細胞移植患者的維持治療研究顯示出良好的應用前景。其他新的聯合治療策略正在臨床研究階段。本文重點回顧AML中已批準和正在研究階段的FLT3抑制劑,包括當前的標準治療和研究策略。
01索拉非尼(sorafenib)
移植后FLT3 TKI維持治療的益處目前仍存在爭議。2018年美國血液學會年會發表的一項隨機研究表明,移植后使用索拉非尼維持治療是有益的。
SORMAIN試驗中,FLT3-ITD突變陽性的AML患者行造血干細胞移植后完全緩解(complete remission ,CR),1:1隨機接受索拉非尼或安慰劑維持治療。研究最終因低累積率而終止,但與安慰劑組相比,索拉非尼治療組患者的2年無復發生存率(relapse-free survival ,RFS)顯著增加,索拉非尼組的無事件生存率(event-free survival ,EFS)為85.0%,而安慰劑組的EFS為53.3%(HR 0.39;95%CI 0.18-0.85;P=0.0135)。
02咪朵妥林(midostaurin)
2017年4月,FDA批準咪朵妥林聯合標準阿糖胞苷和柔紅霉素治療新診斷的FLT3突變陽性的AML患者。研究表明,咪朵妥林聯合化療增加了AML患者的無事件生存率和總生存期。
RATIFY是一項咪朵妥林聯合化療的Ⅲ期臨床試驗,納入717名18-60歲未經治療的FLT3(ITD或TKD)突變陽性的AML患者。患者隨機接受咪朵妥林或安慰劑聯合標準7+3化療,并使用大劑量阿糖胞苷(HiDAC)鞏固治療。鞏固治療后完全緩解的患者使用咪朵妥林或安慰劑維持治療。結果顯示,兩組間的CR率、達到CR的時間無顯著性差異,但咪朵妥林組患者的EFS和總生存期(overall survival, OS)顯著增加。在FLT3突變亞型中的結果一致,包括TKD突變和具有高(>0.7)或低(0.05-0.7)等位基因頻率的ITD突變。此外,在異基因造血干細胞移植(allogeneic hematopoietic stem cell transplantation, allo-HSCT)患者中,兩個治療組也顯示出EFS和OS的差異。因此,咪朵妥林聯合化療已成為新診斷的FLT3突變陽性年輕成年AML患者的新標準療法。
移植后使用咪朵妥林維持治療也是有益的。Radius試驗中, FLT3-ITD突變陽性的成年患者行造血干細胞移植獲得首次完全緩解后,使用咪朵妥林或標準治療(standard of care, SOC)。SOC組和咪朵妥林組的估計復發率分別為24%和11%,咪朵妥林組的復發率相對降低46%。然而,這項研究的組間差異無統計學意義,兩組的RFS中位數也沒有達到。
03奎扎替尼(Quizartinib, AC220)
奎扎替尼是第二代FLT3抑制劑,對野生型LT3和FLT3-ITD突變陽性患者具有更好的療效和選擇性。
一項Ⅱ期臨床試驗評估了2組AML患者:第一組納入難治性AML或年齡>60歲1年內復發的AML患者;第二組納入二線化療或年齡>18歲行HSCT后復發或難治的 AML患者。在該研究中,第1組中56%的FLT3-ITD陽性患者和第二組中46%的FLT3-ITD陽性患者獲得了復合完全緩解(composite CR, CRc)。值得注意的是,接受奎扎替尼治療后實現CRc的FLT3-ITD患者再次復發,可能是由于獲得繼發FLT3-ITD激酶結構域(KD)突變(包含 F691或D835突變)。這一結果表明奎扎替尼是通過靶向抑制FLT3-ITD發揮作用,而不是通過脫靶效應,該研究證實FLT3-ITD是奎扎替尼的一個有效治療靶點。
隨后的一項隨機Ⅱb期研究評估奎扎替尼的2個較低劑量(30或60毫克/天,由于缺乏或失去反應而升級至60或90毫克/天)在76例FLT3-ITD陽性患者中的療效。兩組的CRc發生率均為47%,與使用更高劑量的奎扎替尼觀察到的CRc發生率相似。然而,奎扎替尼低劑量治療的大多數患者并沒有達到CR。低劑量組患者的QT間期發生率低于奎扎替尼高劑量組。在30 mg組和60 mg組患者中,CRc的中位持續時間均較短(4.2w vs 9.1w),且分別有61%和14%的患者出現由于缺乏或失去反應而導致加量的現象。短暫的響應時間和加量現象表明,快速進展的抗藥性是低劑量奎扎替尼治療患者的一個問題。
奎扎替尼(60 mg)與挽救性化療比較的Ⅲ期臨床試驗(QuANTUM-R)結果顯示,與挽救性化療(salvage chemotherapy,SC)相比,使用奎扎替尼治療的FLT3-ITD 陽性的復發/難治(relapsed/refractory ,R/R)AML患者的OS顯著延長。該研究納入18歲以上FLT3-ITD陽性的標準治療后首次復發或難治的AML患者, 2:1隨機接受奎扎替尼或SC方案。在23.5個月的中位隨訪中,奎扎替尼組的中位OS為6.2個月(5.3-7.2個月),而SC組的中位OS為4.7個月(4.0-5.5個月)。奎扎替尼組的移植率較好(32% vs 12%),表明移植率的提高可能是奎札替尼組存活率升高的一個因素。與以前的研究一致,奎扎替尼組的CRc持續時間較短,為12.1周(10.4- 27.1周),且在治療組間的EFS差異不顯著。
奎扎替尼和化療藥物聯合的早期反應率令人鼓舞。一項奎扎替尼聯合誘導鞏固化療的Ⅰ期研究結果顯示,新診斷AML患者的CRi為74%。一項奎扎替尼聯合低甲基化藥物(hypomethylating agent ,HMA)的Ⅰ/Ⅱ期臨床試驗結果顯示,55例FLT3-ITD突變陽性患者的總體響應率為75%,且 5例患者(9%)未檢出微小殘留病(minimal residual disease, MRD)。一項針對不適合化療的FLT3突變陽性AML患者的隨機試驗 (NCT02752035)中,吉列替尼和阿扎胞苷聯合使用的CRc發生率為67%(15例中有10例)。
04吉列替尼(gilteritinib)
2018年11月,FDA批準吉列替尼單藥治療FLT3突變的復發/難治AML患者。研究表明, FLT3突變患者對吉列替尼的響應率較好。
吉列替尼是一種有效的I型FLT3抑制劑,對FLT3 D835突變具有臨床前活性,對FLT3 F691L突變耐藥。一項Ⅰ/Ⅱ期臨床試驗納入252名成年復發/難治AML患者接受吉列替尼治療,結果顯示,191例FLT3突變患者中,70例(37%)患者獲得CRc,大多是接受80毫克/天或更高劑量的患者。值得注意的是,D835突變患者對吉列替尼有應答(應答率低于FLT3-ITD突變患者)。當劑量為80 mg/d或更高時,141例FLT3-ITD突變的患者中有77例(55%)患者出現總體應答(overall responses),12例D835突變患者中的2例(17%)出現總體應答,13例同時存在D835和ITD突變的患者中,8例(62%)患者出現總體應答。
在Ⅲ期ADMIRAL臨床研究中,371例對誘導化療無效或首次復發未治療的FLT3突變(包括ITD和D835/I836突變)AML患者隨機(2:1)接受吉列替尼或挽救性化療(SC)。接受吉列替尼和SC治療患者的OS分別為9.3個月和5.6個月;1年生存率分別為37.1%和16.7%;CR/CRh率分別為34.0%和15.3%;CR率分別為21.1%和10.5%。吉列替尼組的中位反應持續時間為11個月,SC組為1.8個月。重要的是,在FLT3 ITD和TKD 突變患者中觀察到相似的反應率。
吉列替尼聯合化療藥物也顯示出良好結果。一項吉列替尼聯合7+3治療后HiDAC單藥維持治療的Ⅰ期臨床試驗中,17例接受120 mg吉列替尼治療的FLT3突變患者的CRc為100%。接受吉列替尼和柔紅霉素誘導的FLT3突變患者的CRc發生率為100%。在47例接受80毫克吉列替尼治療的患者中,FLT3突變患者的CRc發生率為88.9%(24例)。
05crenolanib
crenolanib是I型FLT3抑制劑,臨床前實驗證實其對FLT3 D835突變具有單藥活性。臨床試驗也證實crenolanib對FLT3突變的復發/難治 AML患者具有單藥活性。
在一項評估crenolanib治療的臨床試驗中,納入18例FLT3突變(6 D835,9 ITD,3 ITD + D835)未使用FLT3 TKI藥物的復發/難治AML患者,crenolanib治療后39%的患者達到Cri,11%的患者達到部分緩解。使用FLT3 TKI治療前進展的36例患者接受crenolanib治療,總體應答率降低為31%(6例CRi, 5例部分應答)。
在一項crenolanib聯合誘導和鞏固化療的臨床試驗中,27例患者中有22例(81%)存活,中位隨訪時間為20.8個月。平均OS、EFS和累計復發發生率尚未達到。
總結
目前,已有3種FLT3抑制劑(索拉非尼、咪朵妥林和吉列替尼)獲FDA批準,其中2種獲批用于AML治療。咪朵妥林聯合化療藥物用于AML患者的一線治療,吉列替尼用于復發/難治的AML患者。另外兩種抑制劑奎扎替尼和crenolanib在AML一線治療和復發/難治患者中的應用處于臨床開發后期階段。
這些藥物在效力、選擇性、半衰期和蛋白結合能力等方面存在差異(見表1),這些特性已在臨床單藥治療中展現出程度不同的獲益。針對FLT3突變的AML患者,最有效的應是強效、選擇性強、生物利用度高,且不易誘發FLT3 KD抗藥性突變的FLT3 TKI藥物。然而,由于個別患者的不良反應導致的耐受性差異,往往會使臨床活性藥物的選擇更為廣泛,正如目前的多種FLT3抑制劑將為新確診和復發AML患者提供更多的治療選擇。
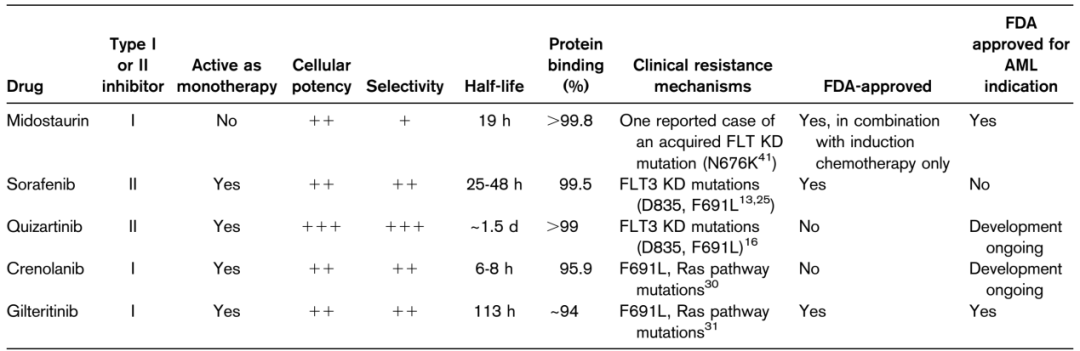
表1 五種FLT3抑制劑的特點
參考文獻
Smith CC. The growing landscape of FLT3 inhibition in AML. Hematology Am Soc Hematol Educ Program. 2019; 2019(1):539-47.