

為了配合新型冠狀病毒肺炎的防控工作,保證實驗室檢測的準確性,2020年2月,蘇州安智因醫學檢驗所參加了由上海市臨床檢驗中心(CNAS PT0025)、上海市臨床檢驗質量控制中心組織的新型冠狀病毒(2019-nCoV)核酸檢測能力驗證項目。收到樣品后,安智因在規定時間內進行了新型冠狀病毒(2019-nCoV)核酸檢測并上報了結果。
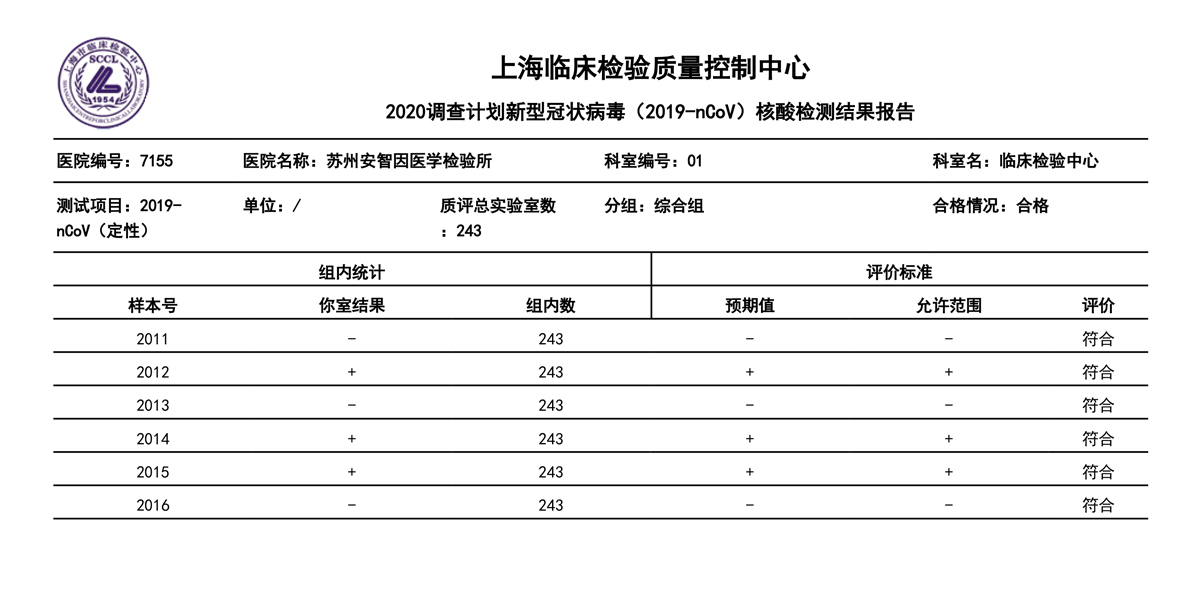
2月22日,蘇州安智因醫學檢驗所收到上海市臨床檢驗質量控制中心發來的室間質評成績報告,報告顯示蘇州安智因醫學檢驗所申請參加的新型冠狀病毒(2019-nCoV)核酸檢測能力驗證的室間質評結果100%符合。
室間質評結果滿分通過,是對蘇州安智因醫學檢驗所檢驗能力的肯定,是安智因檢驗品質和專業度的展現。
蘇州安智因醫檢所基本情況
蘇州安智因醫學檢驗所是安智因生物技術有限公司的全資子公司,位于太倉市經濟技術開發區,總占地面積達1600多平米,是經蘇州市衛生健康委員會核準執業、擁有醫療機構許可資質的第三方獨立醫學實驗室。實驗室嚴格按照《臨床基因擴增檢驗實驗室管理工作導則》進行設計與建設,依托長江三角洲開放區的前沿優勢,逐漸發展為當地醫學檢驗產業的標桿企業。
安智因核心團隊由來自國內外的細胞遺傳學、病理學、分子生物學、以及生物信息分析等領域的專家組成。
蘇州安智因醫學檢驗檢所旨在為臨床提供遺傳病檢測的整體解決方案,檢測服務覆蓋遺傳性心血管病、遺傳性腎病,遺傳性腫瘤,血液病等基因檢測項目,以及個體化用藥指導的基因檢測與感染性病原體檢測等領域。蘇州安智因醫學檢驗所將憑借二代測序檢測及生物信息平臺的技術優勢,為您提供更加精準、完善的檢測服務。